Medizinische Labordiagnostik befasst sich mit der Untersuchung von Körperflüssigkeiten und Körpergeweben auf bestimmte Merkmale und Bestandteile wie Krankheitserreger, Infektionen, Antikörper, Toxine, Gewebestrukturen und Zellentartungen. Der Facharzt für Medizinische und Chemische Labordiagnostik ist Spezialist in diesem Bereich. Wie sieht die Ausbildung zum Facharzt für Medizinische und Chemische Labordiagnostik aus, wo gibt es Beschäftigungsmöglichkeiten und welche (Verdienst-)Perspektiven bestehen? Unser Beitrag beantwortet diese Fragen.
Inhaltsverzeichnis
Facharzt für Medizinische und Chemische Labordiagnostik – Tätigkeiten und Zuständigkeitsgebiet
Wenn auch in Öffentlichkeit weniger präsent, ist Labordaignostik ist ein wichtiges medizinisches Teilgebiet. Patientenkontakt ist hier eher Ausnahme als Regel und die Arbeit findet weitgehend im Hintergrund statt. Dennoch ist Labordiagnostik wichtig und für die Behandlung vieler Erkrankungen unverzichtbar. Etwa zwei Drittel aller ärztlichen Diagnosen beruhen auf Labormedizin.
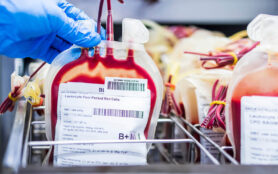
Ärztliche Labordiagnostiker untersuchen Blut, Urin, Fruchtwasser, Abstriche oder Gewebeproben im Hinblick auf ihnen gestellte medizinische Fragen und Prüfaufträge. Sie fassen ihre Ergebnisse in einem Bericht zur Weiterleitung an den behandelnden Arzt zusammen. Der kann darauf seine Therapie aufbauen und weitere Schritte einleiten. In dieser Funktion ist der ärztliche Labordiagnostiker vor allem fachlicher Gutachter. Mehr zu Karriere und Aufgaben in der Fachrichtung hier:
Facharzt für Medizinische und Chemische Labordiagnostik – Die Weiterbildung im Überblick
Wie alle fachärztlichen Ausbildungen in Österreich fußt die Weiterbildung zum Facharzt für Medizinische und Chemische Labordiagnostik auf der Ärzte-Ausbildungsordnung 2015 (ÄAO 2015). Medizinische und Chemische Labordiagnostik bildet ein medizinisches Sonderfach. Die Weiterbildung setzt die allgemeinärztliche Grundausbildung voraus. Ziel der Ausbildung ist, dem angehenden Facharzt die Kenntnisse, Fertigkeiten und Erfahrungen zu vermitteln, die für eine eigenständige und verantwortliche Tätigkeit als ärztlicher Labordiagnostiker erforderlich sind. Die Facharztausbildung wird mit der Facharztprüfung abgeschlossen.
Dauer und Gliederung
Die fachärztliche Weiterbildung ist auf insgesamt 72 Monate angelegt und umfasst drei Abschnitte:
| Abschnitt | Dauer | Inhalte |
|---|---|---|
| Basisausbildung | 9 Monate | Grundkenntnisse Patienten- und Notfallversorgung |
| Sonderfach-Grundausbildung | 27 Monate | Einführung in Verfahren, Qualitätssicherung, Apparatekunde und Infektionsdiagnostik |
| Sonderfach-Schwerpunktausbildung | 36 Monate | Wahlpflicht: 3 aus 6 Modulen + 1 wissenschaftliches Modul |
In der Sonderfach-Schwerpunktausbildung werden sechs fachbezogene Module und ein wissenschaftliches Modul angeboten. Davon müssen drei Module gewählt und belegt werden.
Die 9-monatige Basisausbildung müssen alle angehenden Fachärzte unabhängig von der Fachrichtung absolvieren. Hier erlernen sie grundlegende Kenntnisse der Patienten- und Notfallversorgung, wie sie typischerweise im Krankenhaus vorkommt. Die Basisausbildung findet in der Regel in einem Krankenhaus statt. Dort werden verschiedene Stationen durchlaufen. Den genauen Ablauf legt jedes Krankenhaus selbst fest.
Mehr zu Facharztausbildung und Facharztrichtungen:
- Facharztausbildung Übersicht – alle Fachrichtungen
- Facharztrichtungen – Übersicht
- Internistische Sonderfächer – Übersicht
- Chirurgische Sonderfächer – Übersicht
Inhalte der Sonderfach-Grundausbildung
Die Sonderfach-Grundausbildung gibt einen allgemeinen Überblick über das Fachgebiet und führt in medizinische und chemische labordiagnostische Verfahren ein. Behandelt werden u.a. medizinisch-physikalische Messmethoden einschließlich der chemisch-physikalischen Grundlagen, Untersuchung von Körperflüssigkeiten, Abstrichen und Gewebeproben auf körpereigene und -fremde Inhaltsstoffe und deren Interpretation. Weiterhin umfasst die Sonderfach-Grundausbildung die Vermittlung folgender Kenntnisse, Fähigkeiten und Erfahrungen:
Kenntnisse
- Medizinische und chemische labordiagnostische Verfahren der Präventiv-, Arbeits- und Umweltmedizin und der entsprechenden Erkrankungen
- Geriatrische und pädiatrische Besonderheiten der medizinischen und chemischen Labordiagnostik
- Umwelt- und arbeitsbedingte Risiken und Erkrankungen
- Patientinnen- und Patientensicherheit
- Einschlägige Rechtsvorschriften für die Ausübung des ärztlichen Berufes, insbesondere betreffend das Sozial-, Fürsorge- und Gesundheitswesen, einschließlich entsprechender Institutionenkunde des österreichischen Gesundheitswesens und des Sozialversicherungssystems
- Grundlagen der Dokumentation und Arzthaftung
- Grundlagen der multidisziplinären Koordination und Kooperation, insbesondere mit anderen Gesundheitsberufen und Möglichkeiten der Rehabilitation
- Gesundheitsökonomische Auswirkungen ärztlichen Handelns
- Ethik ärztlichen Handelns
Erfahrungen
- Prävention, fachspezifische Vorsorgemedizin und gesundheitliche Aufklärung
- Allgemeine Medizinische und Chemische Labordiagnostik:
- Grundlagen der Untersuchungsverfahren zur Feststellung physiologischer Eigenschaften sowie der Erkennung und Verlaufskontrolle von Krankheiten des Menschen und die Durchführung der dazu erforderlichen diagnostischen Eingriffe und Funktionsprüfungen
- Interne und externe Qualitätssicherung
- Hygiene
- Grundlagen des Managements eines Laboratoriums
- Tropenmedizin
- Toxikologie
- Anwendung medizinisch-physikalischer Messmethoden sowie die Basis dieser Verfahren der medizinischen Chemie und Physik wie:
- Detektionsverfahren
- Flammenemissionsspektrometrie
- Massenspektometrie
- Quantitative und qualitative Untersuchungen von Körperflüssigkeiten und -proben sowie Gewebe auf körpereigene und fremde Inhaltsstoffe wie Spurenelemente, Toxine und deren Interpretation, Erfahrungen mit Stimulationsversuchen und Belastungstests
- Erfahrungen in Apparatekunde wie technische Funktionsprinzipien von z. B. Pipettier- und Dispensiersystemen, Analysegeräten aus dem Bereich der klinischen Chemie, Hämatologie, Hämostaseologie, Immunologie, Serologie, molekulare Diagnostik, Eingangs-, Funktions-, Richtigkeits- und Präzisionsüberprüfung
- Herstellung und Beurteilung zytologischer Präparate aus Körperflüssigkeiten wie z. B. Harn (mechanisierte Methoden zur Sedimentdiagnostik), Liquor cerebrospinalis
- Grundlagen der diagnostischen Methodik und Beurteilung von Hämoglobinopathien und erythrozytären Defekten
- NA-Analytik aus Tumorzellen
- Testmethodik, Nachweismethoden und in Beurteilung von gerinnungsrelevanter Therapie in Bezug auf Substitution mit Gerinnungsfaktoren
- Transfusionsmedizin: Produktion, Lagerhaltung und therapeutische Verabreichung und Indikation von Blut und Blutprodukten
- Zellpräparative Techniken (wie z. B. zirkulierende Tumorzellen – CTC oder Stammzellen) aus verschiedenen Geweben für Diagnostik und therapeutische Anwendungen
- Methoden der Immunologie wie Spezialelektrophoresen aus allen Körperflüssigkeiten mit niedrigem Proteingehalt
- Basiskompetenz in angewandter Infektionsserologie und Mikrobiologie:
- Färbemethoden für mikroskopischen Erregernachweis
- molekulare Nachweismethoden von Krankheitserregern wie DNA-, RNA-Nachweise
- mikrobiologische Methoden wie Anzüchtung, z. B. Urikult-Identifikation und Empfindlichkeitstestung von Mikroorganismen gegen Antibiotika und Chemotherapeutika aus biologischen Materialien
- Infektionsserologie
- Grundlagen der Antibiotika- und Chemotherapie
- Grundlegende Nachweisverfahren in der Parasitologie
Inhalte der Sonderfach-Schwerpunktausbildung
In der Sonderfach-Schwerpunktausbildung sind folgende 6 Module möglich, aus denen 3 Module gewählt werden müssen.
Modul 1: Blutdepotleitung/Blutgruppenserologie/Hämatologie/Hämostaseologie
- Spenderuntersuchungen: Ausschlussgründe, autologe Blutspende, Apherese, Hygiene der Blutspende und Spendenzwischenfälle
- Physiologie und Immunologie: Physiologie des Sauerstofftransports, Immunologie von zellulären Bestandteilen des Blutes, Stammzellen, hämatopoetische Vorläuferzellen und Gerinnungsphysiologie
- Erfahrungen in HLA-Typisierung
- Zellpräparative Techniken aus verschiedenen Geweben für Diagnostik und therapeutische Anwendungen
- Durchführung der Apherese hämatologischer Zellen
- Beurteilung hämatologischer Zellen mittels molekularer Diagnostik und FISH-Diagnostik
- Beurteilung von chronischen und akuten Leukämien und lymphoproliferative Erkrankungen mittels molekularbiologischer Befunde
- Beurteilung von Hämoglobinopathien
- Bestimmung normaler und abnormer Hämoglobine, weiterführende Untersuchungen wie z. B. molekulargenetische Tests
- Einschätzung des diagnostischen Wertes von bedside-Methoden (hämostaseologisch/hämatologisch)
- Blutgruppenserologie: Einsatz verschiedener blutgruppenserologischer Systeme, Nachweis transfusionsrelevanter Antikörper, Antikörper-Spezifizierung, Durchführung direkter und indirekter Coombs-Tests, Verträglichkeitsproben einschließlich Anwendung molekularbiologischer Diagnostik
- Transport und Lagerung von Blutkomponenten, Durchführung von Qualitätskontrollen sowie Kenntnisse über Zusatzmaßnahmen zur Bearbeitung von Blutprodukten
- Klinische Transfusionsmedizin: interdisziplinäre Indikation von Blutprodukten, Behandlung inkompatibler Transfusionen, Management von Transfusionszwischenfällen und Hämovigilanz
- Qualitätsmanagement in der Transfusionsmedizin
- Leitung eines Blutdepots gemäß gesetzlicher Vorgaben zu Hämovigilanz und Patient-Blood-Management, einschließlich administrativer Aspekte
- Durchführung von Zellzählungen mittels automatisierter Systeme und manueller Kammer bei peripherem Blut, Knochenmark, Punktaten, Stammzellpräparationen und Zellsuspensionen
- Differenzierung mittels automatisierter Systeme und lichtmikroskopischer Befundung bei peripherem Blut, Knochenmark, Stammzellpräparationen und Zellsuspensionen
- Durchführung von Immunphänotypisierungen hämatologischer Zellen
- Bestimmung normaler und abnormer Hämoglobine
- Beurteilung reaktiver Veränderungen sowie verschiedener Formen von Anämie, Leukopenie, Thrombopenie, Polyglobulie/Polyzythämie, Leukozytose, Thrombozytose, Myelodysplasien, akuter und chronischer Leukämien, Lymphomen und lymphoproliferativen Erkrankungen
- Diagnostik und Nachweis von Parasitosen
- Anwendung und Interpretation hämostaseologischer Techniken
- Kontrolle und Bewertung von Antikoagulationstherapien
- Fachspezifische Beurteilung komplexer Gerinnungsstörungen (einschließlich Thrombopathien und Thrombophilien) mit interdisziplinären Therapievorschlägen und molekulargenetischer Diagnostik
Modul 2: Spezielle Klinische Chemie/Immunologie/Molekulargenetik
- Routinemäßiges Arbeiten an automatisierten Analysensystemen
- Immunpathophysiologie: Allergien, Pseudoallergien/Unverträglichkeiten, Autoimmunerkrankungen, Immundefektsyndrome, Transplantationsimmunologie, Tumorimmunologie
- Prinzipien immunologischer Therapien (medikamentöse Immunmodulation, Zytokine/Antizytokine,
- Ig- und Zellersatz) [labormäßiges Therapiemonitoring]
- Prinzipien der Impfung
- Molekularbiologie und Organisation des Genoms, Polymorphismen humaner Gene und posttranslationelle Veränderungen der Genprodukte, Zusammenhang mit anderen Messgrößen und ihre klinische Korrelation
- Etablierung und Leistungsbewertung von molekularen Nachweisverfahren: Verfahren der Nukleinsäureisolierung, Primer- und Sondendesign, Referenzgene und Qualitätskontrollen, Effizienzen und Fehlerraten der reversen Transkription und der Amplifikationstechniken
- Methoden wie z. B. Atomabsorption, Massenspektrometrie – LC-MS oder Tandem-MS
- Medikamenteninterferenz und Medikamenteninteraktion
- Analytische und technische Methodenvergleiche und -evaluation
- MHC-Klasse I und II-Moleküle, Zelloberflächenstrukturen von Leukozyten/Lymphozyten, intrazelluläre Strukturen von Leukozyten/Lymphozyten, Leukozyten-/Lymphozyten-Funktionstests
- Testauswahl: DNA- und RNA-basierte qualitative und quantitative Methoden, Präanalytik, Nachweis von somatischen Mutationen vs. Keimbahnveränderungen, Sensitivitäten/Spezifitäten, Amplifikationseffizienzen, Messunsicherheiten, Nachweisgrenzen/Linearitätsgrenzen, Limitationen der Verfahren
- Techniken wie z. B. FISH, CHIP-Technologie, Sequenzierverfahren
- Aufklärung und fachspezifische Beratung von Patientinnen/Patienten/Probandinnen/Probanden gemäß dem Gentechnikgesetz
- Anfertigung von Metaphasepräparaten aus proliferierenden Kulturen von Patientinnen- und Patientenzellen und anschließender numerischer und struktureller Analyse der Chromosomen nach differentieller Bandenfärbung, differentielle Färbemethoden, Bänderung, Erstellung eines Karyogramms, FISH usw., ISCN-Nomenklatur
- Physikalische, optische und elektrometrische Methoden, Trennmethoden sowie chemische und enzymatische Verfahren zur Bestimmung von Substraten und Enzymaktivitäten
- Immunologische Methoden zur Bestimmung von Hormonen, Medikamentenspiegeln und spezifischen Proteinen
- Durchführung chemischer und morphologischer Harnuntersuchungen
- Klinische Toxikologie und Therapeutic Drug Monitoring
- Nachweis von Suchtmitteln
- Anwendung der Pharmakogenomik und -genetik, insbesondere molekulargenetische Analyse häufiger Polymorphismen mit Relevanz für die Wirkung von Medikamenten und Fremdstoffen
- Durchführung und Bewertung von Qualitätskontrollen und Qualitätssicherungsmaßnahmen, einschließlich interner und externer Verfahren sowie Planung und Umsetzung von Korrekturmaßnahmen
- Adaptierung manueller Methoden oder Fremdreagenzien auf automatisierten Systemen und Analysatoren
- Kenntnis und Anwendung spezifischer Kennzahlen von Testsystemen wie diagnostische Spezifität, Sensitivität sowie positiv- und negativ-prädiktiver Wert
- Bestimmung von Antikörpern, Antigenen und Entzündungsmediatoren durch immunologische Nachweisverfahren (z. B. Line Immunobinding, elektrische Verfahren mit Blotting, Präzipitation, Elektrofokussierung) sowie Anwendung relevanter immunologischer Fachverfahren
- Interpretation immunologischer Faktoren wie Autoantikörper, Ig-Klassen und -Subklassen, spezifische IgE, monoklonale und oligoklonale Immunglobulinveränderungen, Zytokine, Inhibitoren, Adhäsionsmoleküle, Entzündungsparameter, Komplementfaktoren, Kryoglobuline und Immunkomplexe
- Fachspezifische Interpretation molekulargenetischer Befunde
- Befunderstellung gemäß Gentechnikgesetz auf Basis rechtlicher Grundlagen zur genetischen Analyse am Menschen
Modul 3: Infektionsserologie-Mikrobiologie/Labor- und Qualitätsmanagement
- Grundlagen der angewandten Mikrobiologie und Infektionsserologie
- Labor- und Qualitätsmanagement
- Entnahme, Transport und Aufbewahrung von klinischen Proben, Entsorgung von Proben und Labormaterial
- Resistenzbestimmungen, Sequenzierung und Genotypisierung bei viralen Infektionen und deren Therapie
- Optimierung von Arbeitsabläufen, Raumnutzung (Auslastung, räumliche Synergien), Laborgerätenutzung, Nutzung der Laborinfrastruktur, Humanfaktoren (Ergonomie, Arbeitsumgebung)
- Kostenoptimierung durch Synergien, den gesetzliche Grundlagen, der Laborsicherheit, der Etablierung eines Qualitätsmanagementsystems
- Legistik: europäische Direktiven und Richtlinien, nationale Gesetze und Verordnungen, Qualitätsmanagement
- Angewandte Mikrobiologie mit besonderer Berücksichtigung der Infektiologie:
- mikroskopischer Erregernachweis und entsprechende Färbemethoden
- Nachweismethoden von Krankheitserregern wie Antigen- und Antikörper-, DNA-, RNA-Nachweise von HIV-Infektionen, Infektionen mit den Hepatitisviren A, B, C, D, E, Herpesviren, Lues, TORCH, HPV, Bestimmung des viral loads, Genotypisierung, Pilznachweise
- fachspezifische Interpretation spezifischer infektiologischer Befunde inkl. Beratung der klinisch tätigen KollegInnen hinsichtlich weiterführende Diagnostik/ Therapieentscheidungen
- mikrobiologische Methoden wie Anzüchtung, Identifikation von Erregern einschließlich der Mykobakterien, aus klinischen Proben beim Menschen und Empfindlichkeitstestung gegen Antibiotika und Chemotherapeutika aus biologischen Materialien
- immunologischer, serologischer und molekularbiogischer Nachweis von Bakterien und bakterieller Infektionen und Pilzinfektionen, Typisierungsmethoden von Bakterien einschließlich Mykobakterien und Pilzen
- Erstellung der Abwehrlage, Immunitätskontrollen
- Nachweisverfahren in der Parasitologie und Pilzidentifikation
- Befundauswertung aus Serologie und mikrobiologischen Untersuchungen und in der weiterführenden Diagnostik
- Labor- und Qualitätsmanagement
- Beurteilung von Laboruntersuchungen zur Bewertung von ATMP, bezogen auf ATMP-Produkte
- Durchführung von ATMP-Anwendungen oder zugelassenen Anwendungen
Modul 4: Zelluläre Therapie
- Rechtliche Grundlagen: Gentechnikgesetz (GTG), Gewebesicherheitsgesetz (GSG), nationale und übernationale Regulatorien für Advanced Therapy Medicinal Products (ATMP)
- Fachspezifisches Qualitätsmanagement
- Anforderungen an Laboratorien zur Entwicklung und Qualitätssicherung von ATMP
- Anforderungen an Einrichtungen zur Produktion von ATMP
- Zellbiologie unter besonderer Berücksichtigung der Differenzierung und Reprogrammierung
- Epigenetik
- Quellen und Gewinnung von Zellen und Geweben als Ausgangsmaterial für ATMP
- Zell- und Gewebekultur
- Verfahren zur spezifischen Induktion, zur Reprogrammierung und zur genetischen Veränderung im Rahmen der Produktion von ATMP
- Biobanken
- Organisation, Supervision und Qualitätssicherung von Einrichtungen zur Entwicklung, Produktion und Anwendung von ATMP
- Durchführung von ATMP-Anwendungen oder zugelassenen Anwendungen
Modul 5: Transplantationsimmunologie
- Rechtliche Grundlagen der Transplantation in Österreich (Krankenanstalten- und Kuranstaltengesetz, KAKuG)
- Fachspezifisches Qualitätsmanagement: Akkreditierung transplantationsimmunologischer Laboratorien (EFI)
- Organisation des Transplantationswesens (national, international, Widerspruchsregister)
- HLA-System: Bedeutung, Genetik, Gewebeverteilung, Immunologie, Vererbung und Kopplungsungleichgewicht
- ABO-Blutgruppen: Bedeutung für die Transplantation
- Minor histokompatibility antigens: Bedeutung, Genetik, Immunologie, Gewebeverteilung
- Verfahren der Zellisolierung und DNA-Präparation für HLA-Typisierung
- Immunologische Verfahren zur HLA-Typisierung und Antikörperbestimmung
- DNA-Verfahren zur Typisierung von HLA und minor histocompatibility antigens
- Immunologie der Nierentransplantation, Herz, Leber und Lunge
- Spezielle Immunologie der Transplantation von hämatopoetischen Stammzellen (HSC)
- Immunologie der Transplantation anderer Organe nach dem Stand der Entwicklung
- Abstoßungsdiagnostik
- Bedeutung von HLA außerhalb des Transplantationswesens (Krankheitsassoziationen, Pharmakogenomik)
- Organisation eines transplantationsimmunologischen Labors
- Betreuung aller medizinischen Fächer in Fragen der Transplantationsimmunologie
- Bewertung von HLA-Typisierungsergebnissen im Zusammenhang mit Diagnostik HLA-assoziierter Erkrankungen (relatives Risiko) und Pharmokogenomik
- Durchführung von HLA-Klasse I- und II-Typisierungen (low resolution, high resolution) mit akkreditierten Verfahren
- Durchführung von HLA-Antikörperbestimmungen (Klasse I und II) mit akkreditierten Verfahren
- Beurteilung von Typisierungsergebnissen (Plausibilität, Haplotypenzuordnung)
- Durchführung von Crossmatchuntersuchungen vor Transplantation
Modul 6: Diagnostik von Stoffwechselerkrankungen
- Störungen im Aminosäureabbau
- Störungen der Fettsäureoxidation
- Störungen im Harnstoffzyklus, Cholesterinbiosynthese, Gallensäuren
- Lysosomale Erkrankungen
- Peroxisomale Erkrankungen
- Screeningverfahren
- Gaschromatographie-Massenspektrometrie organischer Säuren
- Tandem-MS-Massenspektrometrie
- Lysosomale Erkrankungen: Metabolite (Gruppentests) wie z. B. Mucopolysaccharide, Oligosaccharide und Enzyme wie z. B. Sialidase (Sialidose), lysosomale Hydrolasen (Mucolipidose II, Mucolipidose III), a-Mannosidase (a-Mannosidose)
- Molekulargenetische Analytik – DAN-Mutationsanalysen
- Gaschromatographie-Massenspektrometrie organischer Säuren von z. B. Methylmalonsäure, Pyruvat, Orotsäure
- Photometrische Verfahren wie z. B. Phenylalanin, Kreatin, Mevalonsäure
- Nachweis von z. B. Sterolen, Gallensäuren
Das wissenschaftliche Modul ist fachübergreifend. Es soll auf eine spätere Tätigkeit in Forschung und Lehre vorbereiten. Deshalb werden hier wissenschaftsbezogene Inhalte vermittelt. Es geht u.a. um Techniken des wissenschaftlichen Arbeitens, statistische Methodenlehre, Studienkonzeption und -durchführung, Aufbereitung von Studienergebnissen, Formen der wissenschaftlichen Präsentation und Fragen der Wissenschaftsethik. Bei einer wissenschaftlichen Tätigkeit wird zusätzlich zur Facharztausbildung oft mindestens die Promotion, ggf. auch eine Habilitation erwartet.
Facharztprüfung Medizinische und Chemische Labordiagnostik
Die Facharztprüfung für angehender Labordiagnostiker findet zentral unter Verantwortung der Österreichischen Ärztekammer statt. Es handelt sich um eine strukturiert mündliche Prüfung. Abgeprüft werden zehn bis zwölf Fallbeispiele mit Unterfragen. Die Beispiele sollen praxisnah sein und ein möglichst breites Spektrum der Medizinischen und Chemischen Labordiagnostik abdecken. Prüflinge können sich 30 Minuten auf das Prüfungsgespräch vorbereiten. Um zu bestehen, müssen 70 Prozent der maximal möglichen Punktzahl erreicht sein. Die Facharztprüfung wird “bestanden” oder “nicht bestanden”. Es gibt keine Benotung.
Facharzt für Medizinische und Chemische Labordiagnostik – Lohn
Fachärzte für Medizinische und Chemische Labordiagnostik in Anstellung verdienen in der Regel etwas weniger als Fachärzte in anderen Disziplinen. Laut aktuellen Umfragedaten bewegt sich das Bruttomonatsgehalt in Österreich häufig zwischen 4.080 Euro und 6.810 Euro, abhängig von Berufserfahrung, Funktion und Arbeitgeber.
Dafür bietet der Beruf auch einige “geldwerte” Vorteile. Die Arbeitszeiten sind oft geregelter und die Vereinbarkeit von Familie, Freizeit und Beruf ist eher möglich als bei anderen Facharzttätigkeiten. Bessere Verdienstchancen bestehen beim eigenen Laborbetrieb, allerdings trägt man hier auch das unternehmerische Risiko und das Management erfordert zusätzliche Arbeitskapazitäten. Mehr zum Arzt-Lohn:
Jobs als Labormediziner
Laut offizieller Ärztestatistik 2023 sind in Österreich rund 300 Fachärzte für Medizinische und Chemische Labordiagnostik tätig. Davon arbeiten der Großteil in Anstellungsverhältnissen, ein kleinerer Teil selbstständig. Etwa ein Drittel der Fachärzte verfügt über eine eigene Ordination.
Labormediziner arbeiten überwiegend in Anstellungsverhältnissen. Potentielle Arbeitgeber sind Krankenhäuser, Universitätskliniken, unabhängige medizinische Labore und sonstige Einrichtungen mit medizinischem Laborbetrieb. Daneben besteht aber auch die Möglichkeit, sich selbständig zu machen – mit einem eigenen Laborbetrieb. Das kann als Einzelunternehmen aber auch als Gemeinschaftslabor erfolgen. Hier ist man dann nicht nur als Facharzt, sondern auch als Unternehmer gefragt. Das liegt nicht jedem Mediziner.
Der Bedarf an Labordiagnostik wird in der Zukunft eher größer als kleiner werden. Nicht zuletzt im Zuge der Corona-Pandemie ist deutlich geworden, wie wichtig labormedizinische Erkenntnisse sein können, um Krankheiten zu erkennen, ihre Verbreitung zu bremsen und zielführende Behandlungen durchzuführen. Das gilt selbstverständlich auch für viele andere Krankheitsbilder jenseits von COVID-19. Über mangelnde Beschäftigungsmöglichkeiten dürften sich angehende Fachärzte für Medizinische und Chemische Labordiagnostik jedenfalls nicht beklagen können.
Zukunftsperspektiven Labordiagnostik
Die Nachfrage nach Labordiagnostik wächst stetig. Gründe sind die alternde Bevölkerung, die Zunahme chronischer Erkrankungen, personalisierte Therapien und der Ausbau molekularer Diagnostik. Digitalisierung und Automatisierung werden den Berufsalltag zusätzlich prägen und neue Karrierewege eröffnen.
Passende Stellen
praktischArzt ist die große Jobbörse für Ärztinnen und Ärzte in Deutschland und Österreich. In der Stellensuche sind regelmäßig neue Stellenangebote in allen Facharztrichtungen als Assistenzarzt, Facharzt, Oberarzt und Chefarzt gelistet.
Direkt zu den Jobs für Labormediziner